サイトリニューアルに伴う
ユーザー情報更新のお願い
アプリおよびモバイル端末(iPhone、Android等)の不具合が解消しました。
ICH-GCP(R3)対応につきまして
施設コース案内資料を更新しました
人を対象とする生命科学・医学系研究に関する倫理指針の対応に関しまして
講義の入れ替えや取り下げをすると受講歴に影響するため当面はこのままの掲載としています。順次新指針に合わせた注釈を追加するなどの対応中です。
新指針については、指針本文の確認や 研究倫理指針の解説2023年版、研究倫理指針の解説2022年版を視聴することをお勧めします。
ICRwebからのお知らせ
- 2026年03月24日NEW2026年03月02日2026年02月25日
- 今イチオシの講義 をスキップする
今イチオシの講義
現在人気の講義や今年のトピックの講義です。

0:35:10
分散型臨床試験(Decentralized Clinical Trial;DCT)の基本と計画のポイント《講師:IQVIA サービシーズジャパン合同会社》
世界と日本それぞれにおけるDCTの現状と課題、DCT実施のための検討ポイント、実施方法の基本的な考え方をIQVIAサービシーズ社を招き解説して頂きました。実施医療機関、パートナー医療機関どちらの立場も学べる構成になっています。
閲覧数4
ユーザー評価5.00

0:23:25
治療アプリの開発について《講師:佐竹 晃太》
治療アプリは、医師が処方し、患者が利用するソフトウェアの医療機器であり、従来十分に医療介入できていなかった患者の行動や考え方にアプリで介入し治療します。本講義では、治療アプリの開発をされているCureApp社社長であり医師の佐竹先生を招き、治療アプリの開発や薬事承認、保険償還について解説して頂きました。
閲覧数4
ユーザー評価5.00

0:25:52
臨床研究のQMS体制~それぞれの医療機関で望ましい体制構築へ~《講師:稲田 実枝子》
すべての医療機関が臨床研究中核病院のQMS体制と同じ体制を構築するのではなく、それぞれの医療機関が目指す姿にあわせたQMS体制を構築することが大切です。本講義では、臨床研究中核病院以外の病院の現状・課題に触れ、実地医療に「臨床研究のQMS」を浸透させるための考え方として、医療安全と臨床研究安全について説明しています。すべての医療従事者が医療安全を考えるように臨床研究安全を考えることができれば、自ずと医療と研究の質が向上し、病院として臨床研究のQMS体制が構築されていくと考えます。本コンテンツに関するお問い合わせは、NC・JIHS共通教育講座中央事務局(6nc-educ.jimu@jh.ncgm.go.jp)までご連絡ください。
閲覧数3
ユーザー評価0.00

0:56:35
Estimandの概要とがん臨床試験への適用《講師:水澤 純基》
2024年にICH E9(R1)「臨床試験のための統計的原則 補遺 臨床試験におけるestimandと感度分析」がstep 5となりました。今後、少なくとも治験ではプロトコールにestimandという用語が記載され、この用語を用いて試験の目的が整理されるようになります。この流れは研究者主導臨床試験においても避けられず、近い将来、各臨床試験のプロトコールにも漏れなく記載されることになります。研究者・研究支援者(CRC、DM、CRA、PMなど)が知っておくべきestimandの概念について解説しました。わかりやすさのために一部正確さを犠牲にしているところがありますので、詳しくはガイドラインやトレーニングマテリアルを参照ください。
閲覧数193
ユーザー評価4.53

0:02:45
第1章 RBA実践の前準備
本章では、RBAを実装するための準備段階として、基本的な概念の解説と各種資料やツールの紹介を行いました。RBAではRBA自体の理解だけでなく、RBAを実践する体制やプロセスを含めて準備することが重要です。各資料を活用しながら適切に準備を進めてください。 次の章では、CTQ(Critical to Quality)の特定とリスクの特定について詳しく解説します。CTQの考え方を理解し、適切なリスク管理を行うためのフレームワークを紹介します。 1_RBA手順の実践ガイド.pdf 2_リスク管理表記載ナビ.pdf 3_IQRMPにおける治験関連文書一覧.pdf 4_リスクカテゴリ参考資料.pdf 5_責任分担表の作成.pdf 6_コミュニケーションマネジメント.pdf 7_多職種コンピテンシー.pdf 8_RBAにおける多職種の視点.pdf 14_経験学習モデル.pdf 15_KPTシート.xlsx 18_リスク報告例.pdf
閲覧数68
ユーザー評価0.00

0:47:09
GCP Basicトレーニング《講師:古谷秀樹》
本講義では、GCP(Good Clinical Practice)に関する基本的な知識を解説しています。医薬品開発の流れ、関連法規、GCP省令の構成、治験に関わる各職種の役割、インフォームド・コンセントの取得方法、有害事象の報告、記録の保存などを網羅的に説明し、近年の治験のデジタル化やDCT(分散型臨床試験)の事例も紹介しています。本コンテンツに関するお問い合わせは、NC・JIHS共通教育講座中央事務局(6nc-educ.jimu@jh.ncgm.go.jp)までご連絡ください。
閲覧数390
ユーザー評価4.30

0:43:53
臨床研究法の改正について《講師:飯村康夫》
本講義は臨床研究法の改正に関する解説であり、過去の不正事例を背景に、研究の信頼性と透明性を確保するための制度整備を紹介しています。特定臨床研究の定義や手続き、認定審査委員会の役割、利益相反管理、研究対象者の保護などが詳述され、法施行5年後の見直し内容や今後の課題も示されています。本コンテンツに関するお問い合わせは、NC・JIHS共通教育講座中央事務局(6nc-educ.jimu@jh.ncgm.go.jp)までご連絡ください。
閲覧数391
ユーザー評価4.47

0:58:33
改正臨床研究法 ①研究対象者に著しい負担を与える検査等の考え方 ②特定臨床研究から除外できる適応外使用の考え方《講師:①佐藤典宏 ②布施望》
①の講義では、臨床研究法の改正に伴う「著しい負担を与える検査等」の定義と判断基準を中心に、観察研究との区別や具体的事例を通じて、法適用の妥当性を検討しています。②の講義では、特定臨床研究から除外される「適応外使用」に関する基準や事例を整理し、CRBによる審査の在り方や今後の制度運用の方向性を示しています。本コンテンツに関するお問い合わせは、NC・JIHS共通教育講座中央事務局(6nc-educ.jimu@jh.ncgm.go.jp)までご連絡ください。
閲覧数184
ユーザー評価4.32

0:45:32
臨床研究とは~治験と臨床研究の違いについて~《講師:布施望》
本講義では、がん領域における臨床研究と治験の違いを中心に、関連する法令(薬機法、臨床研究法、安確法、倫理指針)や制度、手続き、書式の違いについて体系的に解説しています。また、医薬品・医療機器・再生医療等製品の安全性・有効性評価に関する実務的知識についても紹介しています。本コンテンツに関するお問い合わせは、NC・JIHS共通教育講座中央事務局(6nc-educ.jimu@jh.ncgm.go.jp)までご連絡ください。
閲覧数755
ユーザー評価4.20
0:25:20
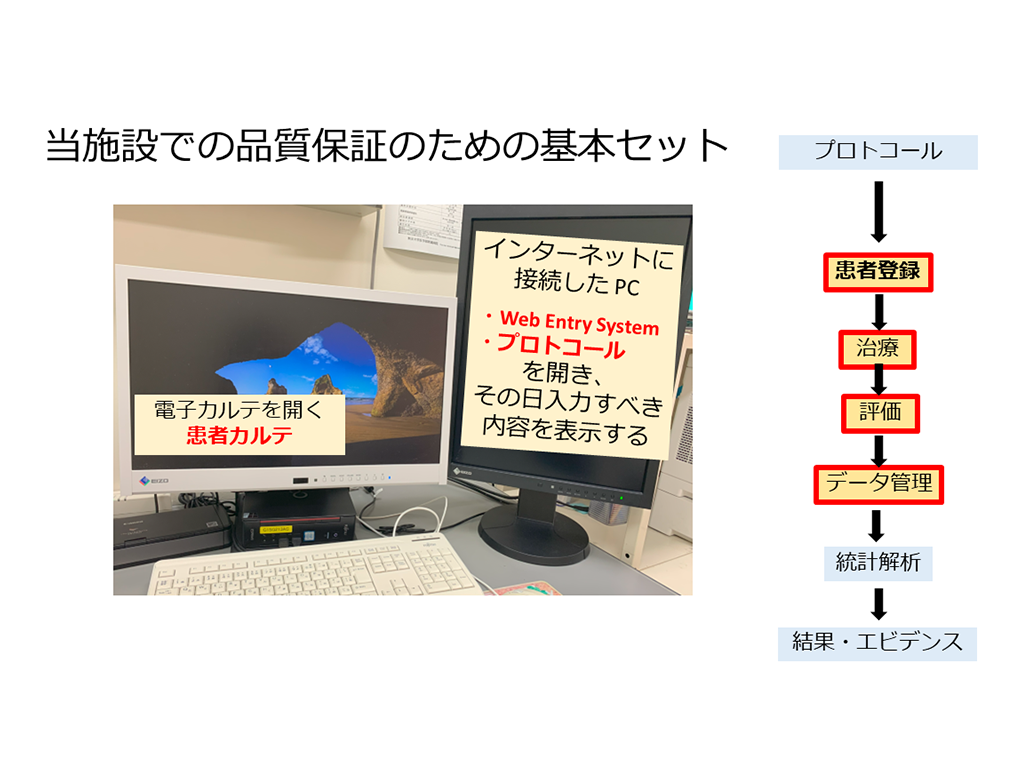
当院における品質保証の工夫《講師:寺田 かおり》
研究者主導臨床試験では必ずしもCRCなどの支援を受けられず、研究者自身が同意取得、文書管理、プロトコールの確認、EDCへの入力/CRF記載をしている場合も多いかと思います。そのようにリソースが限られる中で、どのような事が可能なのか、JCOG参加施設の医療機関に対する監査の結果が非常に良かった秋田大学乳腺・内分泌外科の取り組みをお話しいただきました。是非、御自身の施設でも真似してみてください。
閲覧数8644
ユーザー評価4.18
‹›
スタンダード必修コース
この講座は、臨床研究の基本を理解し、臨床研究を実施する際に必要な最低限の知識を得ることを目的としており、臨床研究に携わるすべての人が知っておくべき基礎的な内容です。他の講義のエッセンスをできるだけ網羅的に集めましたので、本講座を受講して臨床研究の全体像を把握してください。
0:08:51
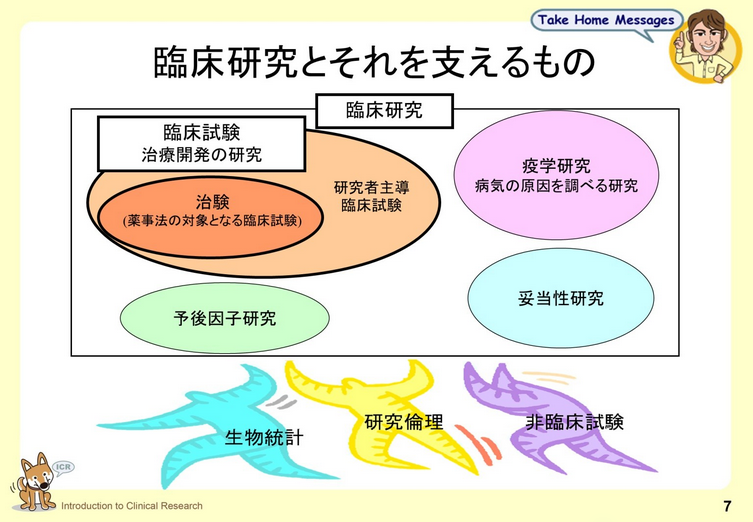
1. 臨床研究概論
臨床研究の分類とそれぞれの具体例を紹介し、臨床研究の全体像を大まかに把握することを目的としています。
閲覧数140152
ユーザー評価4.22
0:36:54
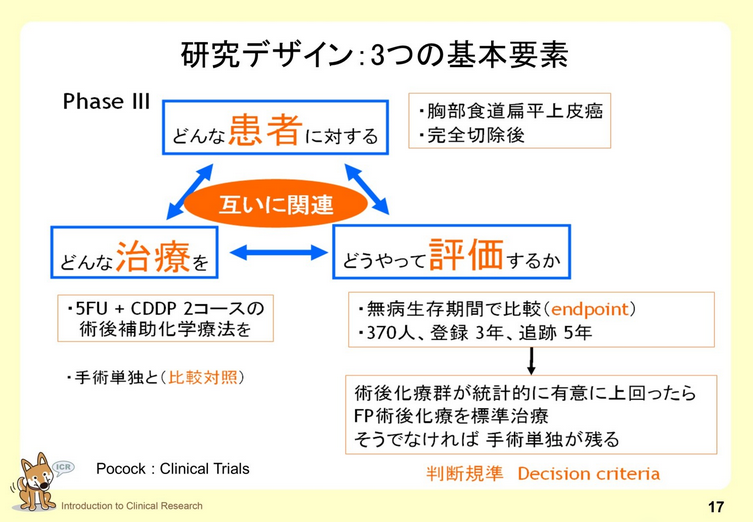
2. 治療開発のための研究1:臨床試験
治療開発のための研究として、臨床試験による治療開発について説明しています。
閲覧数129500
ユーザー評価4.22
0:35:21
3. 治療開発のための研究2:非臨床試験
医薬品開発のために必要な研究として、非臨床試験による安全性評価について説明しています。
閲覧数116317
ユーザー評価4.11
0:19:31
4. 治療開発のための研究3:治験
治療開発の重要なステップとして、医薬品の治験について解説し、>新薬が世に出るまでの流れを説明しています。
閲覧数113306
ユーザー評価4.04
0:15:48
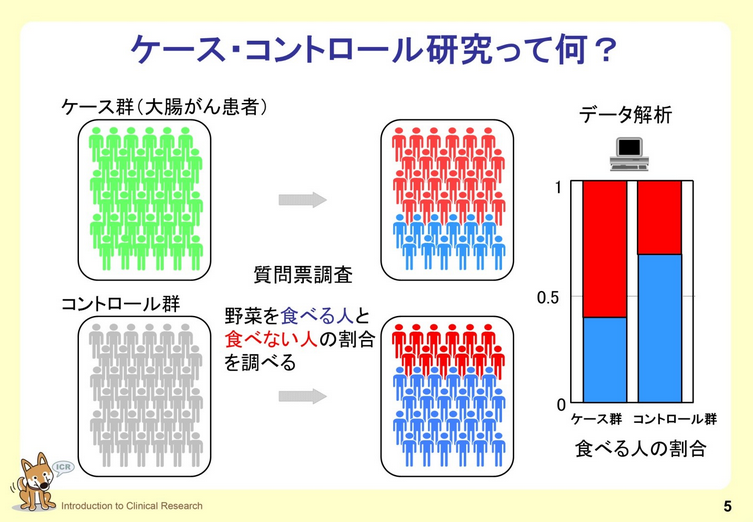
5. 病気の原因を調べるための疫学研究1:ケース・コントロール研究
観察研究によって病気の原因を探索するための因果推論の方法として、疫学研究デザインの1つであるケース・コントロール研究の説明をしています。
閲覧数112379
ユーザー評価4.11
0:17:32
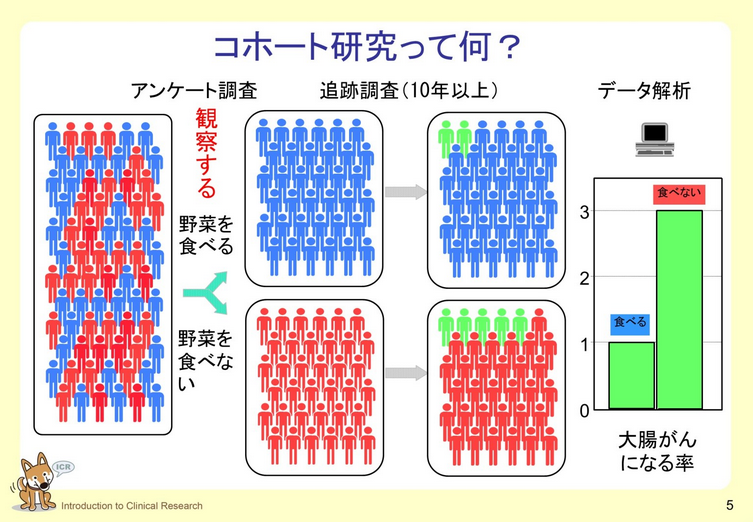
6. 病気の原因を調べるための疫学研究2:コホート研究
観察研究によって病気の原因を探索するための因果推論の方法として、代表的な疫学研究デザインである「コホート研究」について、「ケース・コントロール研究」と比較しながら説明しています。
閲覧数110956
ユーザー評価4.11
0:16:27
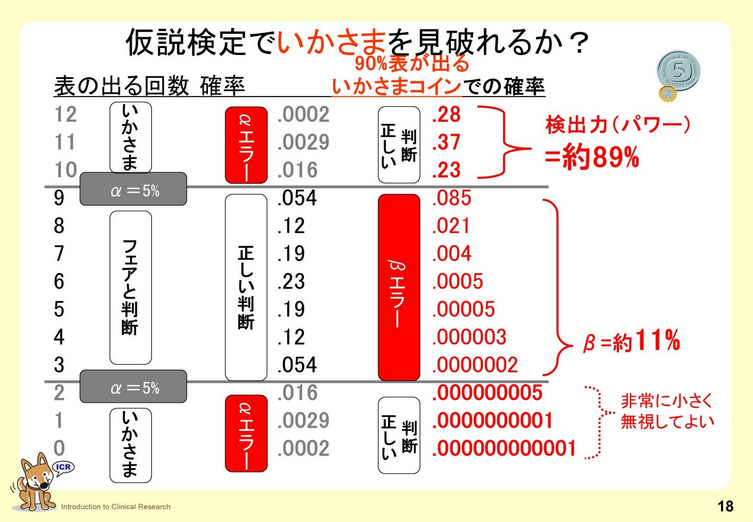
7. 生物統計学1:仮説検定
臨床研究にかかわる上で知っておく必要のある生物統計学の概念と仮説検定について説明しています。
閲覧数110954
ユーザー評価4.13
0:15:38
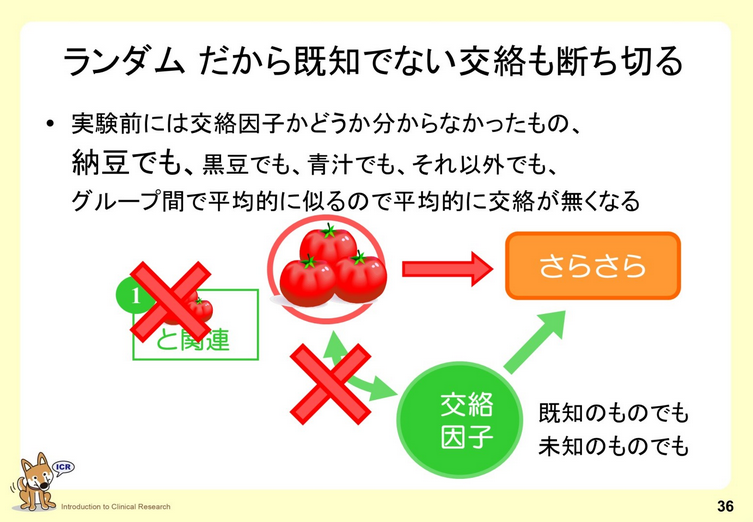
8. 生物統計学2:交絡・ランダム化と因果推論
臨床研究を支える生物統計学の中で、因果推論をする際の重要な概念である交絡とその調整、ランダム化について説明しています。
閲覧数109278
ユーザー評価4.14
0:26:22
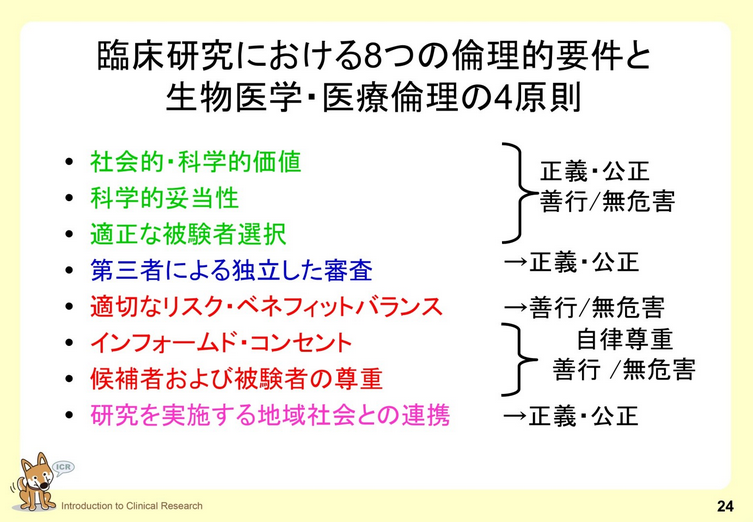
9. 研究倫理と被験者保護
臨床研究に参加する被験者の権利と福利を保護し、かつ安全性を確保するために払うべき倫理的配慮、すなわち被験者保護を実践するために、研究倫理の基本概念を説明しています。
閲覧数116500
ユーザー評価4.12

0:38:18
10.「人を対象とする医学系研究に関する倫理指針」の解説
人を対象とする医学系研究に関する倫理指針の解説を田代先生に講義頂きました。鍵となる概念「介入と侵襲」についてもわかりやすく解説していただきました。指針の細かい解釈に陥ることなく、その本質を理解するためにぜひ履修してください。
閲覧数94958
ユーザー評価4.13
‹›
新着講義
最近公開した講義を集めました。

0:23:25
治療アプリの開発について《講師:佐竹 晃太》
治療アプリは、医師が処方し、患者が利用するソフトウェアの医療機器であり、従来十分に医療介入できていなかった患者の行動や考え方にアプリで介入し治療します。本講義では、治療アプリの開発をされているCureApp社社長であり医師の佐竹先生を招き、治療アプリの開発や薬事承認、保険償還について解説して頂きました。
閲覧数4
ユーザー評価5.00

0:46:35
試験デザインに必要な生物統計の基礎知識《講師:若林 将史》
国立がん研究センター 研究支援センター 生物統計部の若林将史医学統計室長に、臨床試験デザインを検討するポイントの中から、群間比較試験で用いられることが多いランダム化における注意点、目標症例数の設定。また、試験結果に出てくるp値の意味や解釈する際の注意点を取り上げ、詳しく解説頂きました。
閲覧数4
ユーザー評価5.00

0:35:10
分散型臨床試験(Decentralized Clinical Trial;DCT)の基本と計画のポイント《講師:IQVIA サービシーズジャパン合同会社》
世界と日本それぞれにおけるDCTの現状と課題、DCT実施のための検討ポイント、実施方法の基本的な考え方をIQVIAサービシーズ社を招き解説して頂きました。実施医療機関、パートナー医療機関どちらの立場も学べる構成になっています。
閲覧数4
ユーザー評価5.00

0:49:13
DCTを実施するための体制作り 日本の強みを活かす実践的アプローチ《講師:船越 公太》
DCT実施体制や医療環境の背景について、海外と日本との国際比較を通し、海外で行われている仕組みをそのまま日本で行うのではなく、日本に適したDCTの仕組みはどういうものがあるのか。DCTを推進されている九州大学 船越先生を招き解説して頂きました。
閲覧数3
ユーザー評価5.00

0:48:34
DCTを実現するために必要な手段やツールについて《講師:浅野 健人》
DCTを実現するために必要な手段やツール、工夫を、多くのDCTを実践されている大阪大学 浅野先生を招き、実施された臨床試験3試験を題材に解説して頂きました。
閲覧数2
ユーザー評価5.00

0:25:52
臨床研究のQMS体制~それぞれの医療機関で望ましい体制構築へ~《講師:稲田 実枝子》
すべての医療機関が臨床研究中核病院のQMS体制と同じ体制を構築するのではなく、それぞれの医療機関が目指す姿にあわせたQMS体制を構築することが大切です。本講義では、臨床研究中核病院以外の病院の現状・課題に触れ、実地医療に「臨床研究のQMS」を浸透させるための考え方として、医療安全と臨床研究安全について説明しています。すべての医療従事者が医療安全を考えるように臨床研究安全を考えることができれば、自ずと医療と研究の質が向上し、病院として臨床研究のQMS体制が構築されていくと考えます。本コンテンツに関するお問い合わせは、NC・JIHS共通教育講座中央事務局(6nc-educ.jimu@jh.ncgm.go.jp)までご連絡ください。
閲覧数3
ユーザー評価0.00

0:35:47
脳卒中急性期臨床試験におけるQMS/RBA実装の試み《講師:福田 真弓》
本講義では、前回ご紹介した臨床試験におけるQMS/RBA実装の取り組みを振り返りつつ、その後の運用を通じて見えてきた課題や工夫、得られた示唆について後日談的にお話しします。実際の試験進行の中で明らかになったポイントを共有することで、今後の品質管理実践の一助となれば幸いです。本コンテンツに関するお問い合わせは、NC・JIHS共通教育講座中央事務局(6nc-educ.jimu@jh.ncgm.go.jp)までご連絡ください。
閲覧数2
ユーザー評価0.00

0:36:23
QbDは試験開始時だけじゃない!~解析対象集団の決定を見据えたRisk Based Approachの展開《講師:山田 知美》
本講義では、Quality by Designを試験開始時の設計に留めず、試験中に発生する逸脱を統計学的にどのように捉え、扱うかを解説します。治療効果を評価する対象(Estimand)を軸に、「症例採否やデータの取扱い」が治療効果評価に与える影響を整理し、重要な逸脱・欠測を品質リスクとして管理する方法を示します。さらに、QTL(品質許容限界)の設定と中央モニタリングを通じて継続的に確認・是正する、QbD/Risk Based Approachの実践的な考え方を学びます。本コンテンツに関するお問い合わせは、NC・JIHS共通教育講座中央事務局(6nc-educ.jimu@jh.ncgm.go.jp)までご連絡ください。
閲覧数1
ユーザー評価0.00

0:24:50
自己署名証明書を利用し暗号化通信を実装したウェブサイトを構築《講師: 岡村浩司》
ウェブサーバとブラウザとの通信は現在ではほとんどが暗号化され、盗聴、中間者攻撃などから守られ、なりすましや偽サイト、フィッシング詐欺等の対策がなされています。これを実現しているのがTLSを利用したサーバ証明書ですが、気軽に試すことが困難です。今回、自己署名証明書を作成、暗号化通信を実装したウェブサーバを構築し、セキュリティの観点から重要な証明書について理解を深めたいと思います。この動画は第262回データサイエンス研修にて発表された内容を再収録したものです。本コンテンツに関するお問い合わせは、NC・JIHS共通教育講座中央事務局(6nc-educ.jimu@jh.ncgm.go.jp)までご連絡ください。
閲覧数1
ユーザー評価0.00

0:34:52
統計学的基礎知識②多重検定問題と分散分析《講師:中林 潤》
仮説検定を複数回繰り返すことを多重検定と言いますが、ここではまず多重検定を行う際の問題点を説明します。バイオインフォマティクス解析では大量のデータを扱うので、多重検定が避けられません。そこで、多重検定の対処方法についても解説します。本コンテンツに関するお問い合わせは、NC・JIHS共通教育講座中央事務局(6nc-educ.jimu@jh.ncgm.go.jp)までご連絡ください。
閲覧数1
ユーザー評価0.00

0:38:07
統計学的基礎知識③多次元データと次元縮約《講師:中林 潤》
バイオインフォマティクス解析では高次元のデータを頻繁に扱います。ここでは多次元データの処理方法や、高次元のデータを低次元に縮約する次元縮約の理論と方法を解説していきます。本コンテンツに関するお問い合わせは、NC・JIHS共通教育講座中央事務局(6nc-educ.jimu@jh.ncgm.go.jp)までご連絡ください。
閲覧数1
ユーザー評価0.00

0:47:16
知的財産セミナーシリーズ4 医療情報の取扱いに関する留意点《講師:JH知財・法務課》
医療ライフサイエンス研究者が知っておくべき医療情報の取扱いに関する留意点について4つの要点(①次世代医療基盤法の基礎知識 ②個人情報保護法と第三者提供のルール ③医学系指針(ヒト指針)と倫理 ④研究責任者のガバナンスと事例)に分け、わかりやすく解説しています。 この動画は、ナショナルセンター医療研究連携推進本部(Japan Health Research Promotion Bureau:JH)知財・法務課が作成しました。本コンテンツに関するお問い合わせは、NC・JIHS 共通教育講座中央事務局(6nc-educ.jimu@jh.ncgm.go.jp)までご連絡ください。
閲覧数1
ユーザー評価0.00
‹›
ピックアップ:倫理指針・規制要件
頻繁に更新される倫理指針や2018年に施行された臨床研究法。過去の講義から順にみて頂くのが改訂の経緯も含めて最も理解が深まりますが、最低限これだけは、というものを集めました。

0:47:09
GCP Basicトレーニング《講師:古谷秀樹》
本講義では、GCP(Good Clinical Practice)に関する基本的な知識を解説しています。医薬品開発の流れ、関連法規、GCP省令の構成、治験に関わる各職種の役割、インフォームド・コンセントの取得方法、有害事象の報告、記録の保存などを網羅的に説明し、近年の治験のデジタル化やDCT(分散型臨床試験)の事例も紹介しています。本コンテンツに関するお問い合わせは、NC・JIHS共通教育講座中央事務局(6nc-educ.jimu@jh.ncgm.go.jp)までご連絡ください。
閲覧数390
ユーザー評価4.30

0:43:53
臨床研究法の改正について《講師:飯村康夫》
本講義は臨床研究法の改正に関する解説であり、過去の不正事例を背景に、研究の信頼性と透明性を確保するための制度整備を紹介しています。特定臨床研究の定義や手続き、認定審査委員会の役割、利益相反管理、研究対象者の保護などが詳述され、法施行5年後の見直し内容や今後の課題も示されています。本コンテンツに関するお問い合わせは、NC・JIHS共通教育講座中央事務局(6nc-educ.jimu@jh.ncgm.go.jp)までご連絡ください。
閲覧数391
ユーザー評価4.47

0:58:33
改正臨床研究法 ①研究対象者に著しい負担を与える検査等の考え方 ②特定臨床研究から除外できる適応外使用の考え方《講師:①佐藤典宏 ②布施望》
①の講義では、臨床研究法の改正に伴う「著しい負担を与える検査等」の定義と判断基準を中心に、観察研究との区別や具体的事例を通じて、法適用の妥当性を検討しています。②の講義では、特定臨床研究から除外される「適応外使用」に関する基準や事例を整理し、CRBによる審査の在り方や今後の制度運用の方向性を示しています。本コンテンツに関するお問い合わせは、NC・JIHS共通教育講座中央事務局(6nc-educ.jimu@jh.ncgm.go.jp)までご連絡ください。
閲覧数184
ユーザー評価4.32

00:26:23
2023年7月施行の改訂研究倫理指針について《講師:一家綱邦》
2023年時点の「人を対象とする生命科学・医学系研究に関する倫理指針」(令和5年3月27日一部改正)の解説に関して、改正点を中心に解説しています。研究倫理の成り立ちや指針の基本的な考え方についてはリンク先の講義を視聴することをおすすめいたします。
閲覧数20235
ユーザー評価4.23

0:39:46
人を対象とする生命科学・医学系研究に関する倫理指針《講師:遠矢和希》
「ヒトゲノム・遺伝子解析研究に関する倫理指針」及び「人を対象とする医学系研究に関する倫理指針」を統合し、2021年3月23日に新たに制定された「人を対象とする生命科学・医学系研究に関する倫理指針」をはじめ、日本における臨床研究規制について幅広く解説頂きました。
閲覧数8320
ユーザー評価4.30

00:37:34
先進医療・患者申出療養とは《講師:安藤弥生》
先進医療・患者申出療養とはどういうものか、保険外併用療法等の制度面の説明に加えて、実例2例を紹介しています。2023年8月8日に行われました国立がん研究センターの臨床研究関連セミナーを収録したものです。本コンテンツに関するお問い合わせは、6NC共通教育講座中央事務局(6nc-educ.jimu@jh.ncgm.go.jp)までご連絡ください。
閲覧数276
ユーザー評価4.36

0:45:32
臨床研究とは~治験と臨床研究の違いについて~《講師:布施望》
本講義では、がん領域における臨床研究と治験の違いを中心に、関連する法令(薬機法、臨床研究法、安確法、倫理指針)や制度、手続き、書式の違いについて体系的に解説しています。また、医薬品・医療機器・再生医療等製品の安全性・有効性評価に関する実務的知識についても紹介しています。本コンテンツに関するお問い合わせは、NC・JIHS共通教育講座中央事務局(6nc-educ.jimu@jh.ncgm.go.jp)までご連絡ください。
閲覧数755
ユーザー評価4.20
‹›
ピックアップ:研究倫理・研究不正
臨床研究を行うためにすべての方が必要な研究倫理に関する必須講義をまとめました。なぜIRBの審査・承認が必要なのか。臨床研究に関する歴史と犠牲から研究倫理の本質を理解してください。

00:36:56
研究倫理ベーシック 《講師:田代志門》
人を対象としておこなう医学系研究に共通する倫理面の3つの重要なトピックである研究対象者の保護 、研究不正の防止、 利益相反の管理 について講義していただきました。 臨床研究を行う研究者・支援者すべての人が受講必須の内容です。
閲覧数6952
ユーザー評価4.25
0:52:32
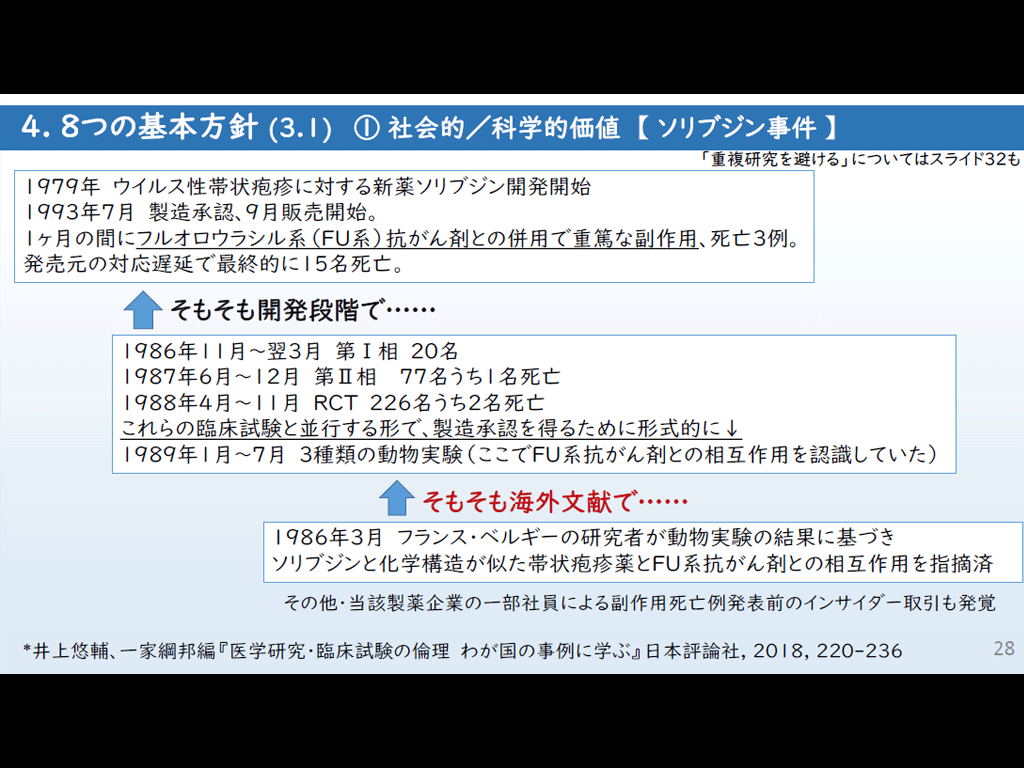
研究倫理の成り立ち 歴史と基本《講師:遠矢和希》
臨床研究の実施前に、なぜIRBの審査・承認が必要なのか。本講義では、米国のタスキギー事件、日本のソリブジン事件などを例として、臨床研究に関する歴史と犠牲から研究倫理及びIRB審査の必要性を解説します。
閲覧数3477
ユーザー評価4.38
00:58:56
研究不正、企業不正の背景を考える 《講師:黒木登志夫》
本講義では日本学術振興会の黒木登志夫先生に、研究不正の基本的事項、発生背景、および再発防止策について、データ分析と具体的事例を豊富に盛り込んで解説いただきました。(平成29年2月11日 第2回研究倫理を語る会にて収録)
閲覧数4708
ユーザー評価4.33
‹›
ピックアップ:生物統計入門
苦手意識のある方も多い統計学。まずはこのあたりからトライしてみてはいかがでしょうか。
01:07:01
データの記述 《講師:水澤純基》
普段、年齢や検査値などの連続量データを要約する際は、とりあえず中央値と範囲を出すものだと思っていませんか?なぜ平均値ではないか説明できるでしょうか?本講義では、ヒストグラムや散布図などを使ったデータの解釈や解析法の選択など、基礎的な内容であるがゆえに今まで誰も教えてくれなかった内容について解説します。本講義では検定や推定を実施する前に行うべきデータクリーニングや予備的解析についても説明します。ぜひ、履修してください。
閲覧数16689
ユーザー評価4.37
00:42:49
仮説検定1 《講師:口羽文》
本講義では統計学的仮説検定についての基礎を説明します。 論文・学会発表ではp値を必ず目にしますが、 p値の定義・考え方を正確に理解していますか? 是非、本講義を通して自分で説明できるようになってください。
閲覧数9745
ユーザー評価4.19
00:48:49
仮説検定2 《講師:口羽文》
第2回は、連続量、カテゴリカルデータがアウトカムである場合を取り上げます。 「連続量で数が少ないとWilcoxon検定」、「カテゴリカルデータで数が少ないとFisher検定」などと安易に決めつけてはいませんか? 本講義では、適切な検定の考え方を説明いたします。
閲覧数7392
ユーザー評価4.23
01:06:20
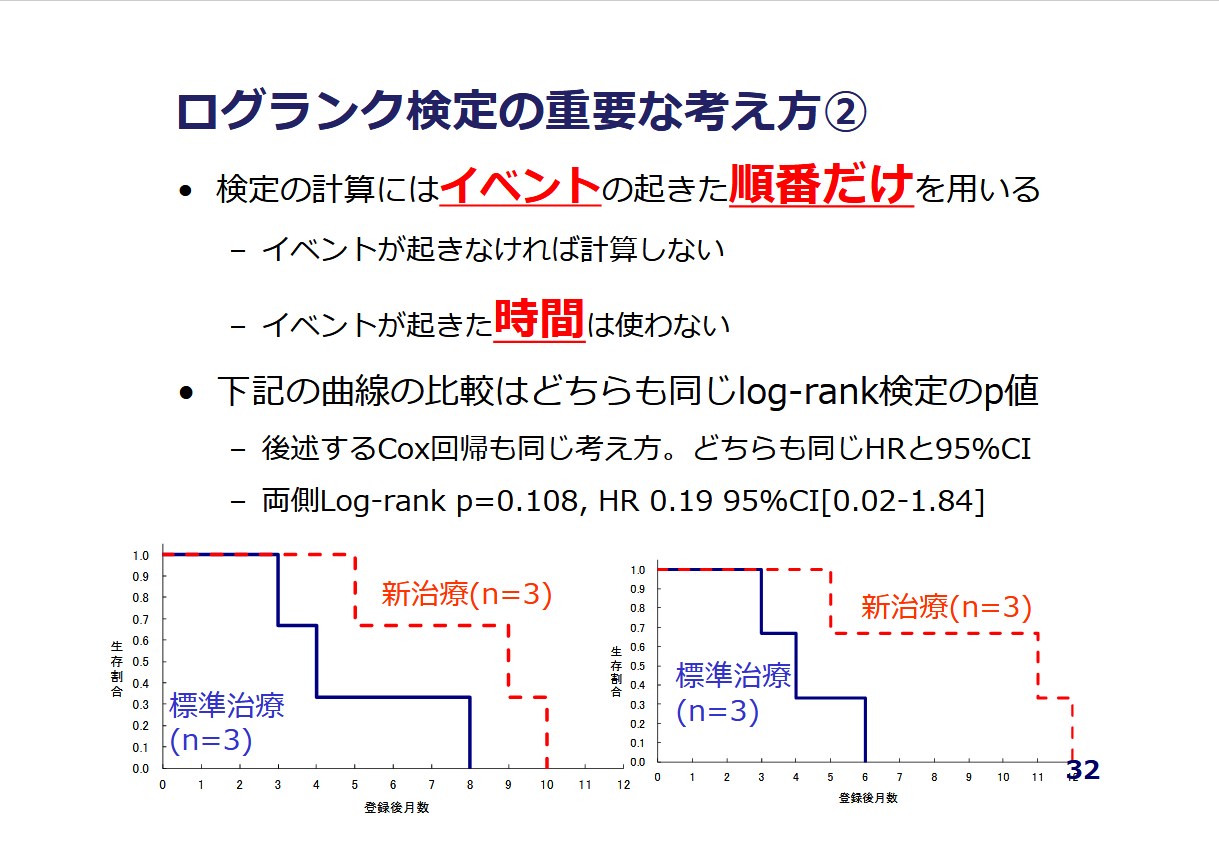
生存時間解析 《講師:水澤純基》
がんの臨床研究において特に重要な解析手法である生存時間解析について説明します。アウトカムが生存時間の場合,また別の解析手法が必要となります。 一体なぜ連続量・ カテゴリカルデータに対する解析手法を用いることが適切ではないのでしょうか? 本講義を 通して生存時間解析の基本的な考え方を身につけてください。
閲覧数6971
ユーザー評価4.41
00:52:46
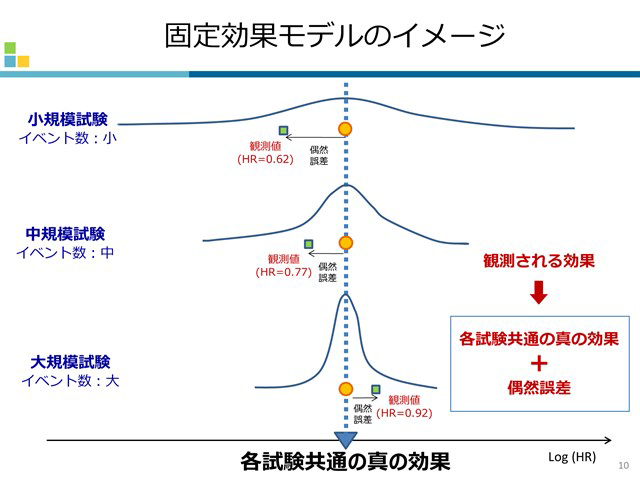
メタアナリシス入門 《講師:山中竹春》
メタアナリシスは、複数の試験を“ひとつのハザード比(or オッズ比 etc)”に要約してしまうことから、その結果が意味するところは非常に単純明快で、EBMの普及にも一定の貢献を果たしてきたと思います。 今回はメタアナリシスの基本的な方法論、そして、メタアナリシスが本当にレベル1Aのエビデンスかどうかを皆さんと一緒に考えたいと思います。
閲覧数2486
ユーザー評価4.20
‹›
ピックアップ:PPI
はじめて学ぶ「研究への患者・市民参画」

この講座は、研究への患者・市民参画(PPI:Patient and Public Involvement)について、初めてPPIを学ぶ人が基本的な知識を得ることを目的としています。この講座では、PPIの考え方、PPI活動をする上で必要になる基本的知識、PPI活動でのコミュニケーションの方法やこれらの注意点について学ぶことができます。その上で、研究のさまざまな段階で行われるより具体的なPPI活動に関する知識を学ぶことができます。この講座は、AMED「治験・臨床研究における患者・市民参画を推進する手法の確立」(東京大学・武藤香織)により製作され、一般社団法人PPI Japanにより運営されています。
日本対がん協会公開講座-臨床試験を身近に-

臨床試験と治験は何が違うのか、ガイドラインに掲載される標準治療と臨床試験の違いは何なのか。一般的に難しく思われがちな「臨床試験」や「治験」について、より深く知り身近に感じていただくことを目的に、実際に臨床試験に関わる医師や、参加した患者さんの体験談を合わせ、わかりやすくお伝えいたします。 近年、新薬の登場などで大きく進歩しているがん治療。既存の薬や治療法との組み合わせを含めた、より有効な治療法を確立するために、いま臨床試験の重要性が高まっています。患者、そして市民がともに未来のがん治療を“共創”する時代へ。がん医療の専門家と一緒に、臨床試験や「患者・市民参画」の大切さを一緒に考えてみませんか? この講座は公益財団法人日本対がん協会と日本臨床腫瘍研究グループ(JCOG)共催の公開講座です。
第3回JCOG患者・市民セミナープログラム
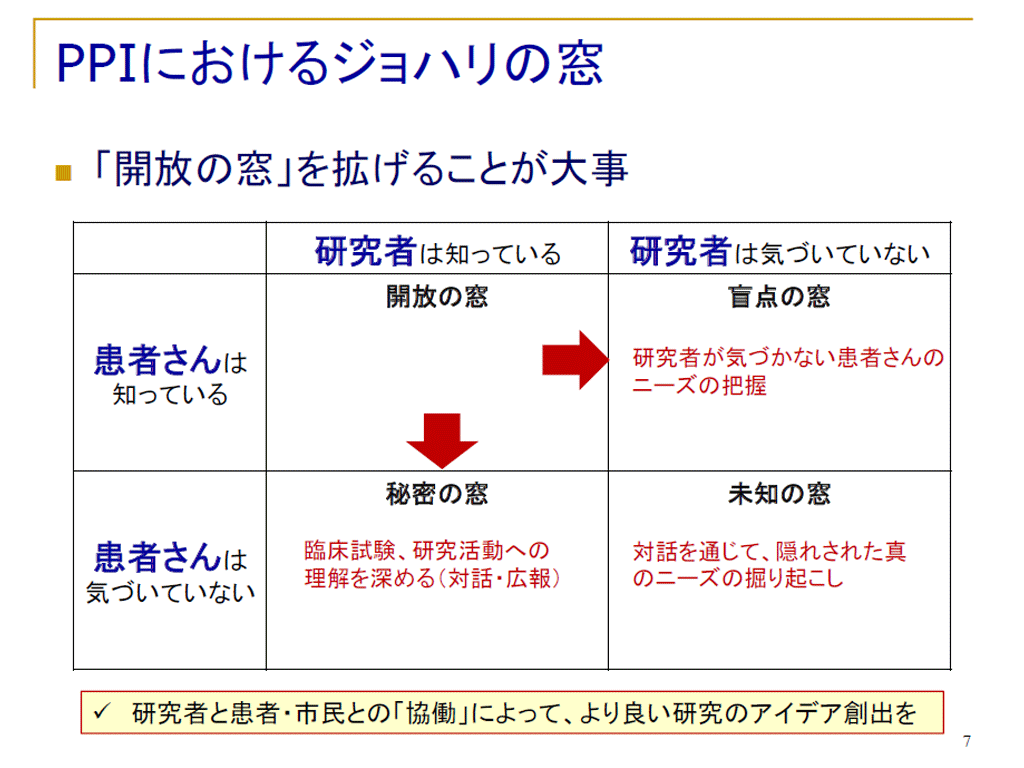
近年、医学研究・臨床試験における患者・市民参画(PPI,Patient and Public Involvement)の取り組みが広がりつつあります。何の事かわからないという方も、興味はあるけどどのように初めていけばわからないという方も、がんを対象とした多施設共同臨床研究グループのJCOGの取り組みを参考に、まずは始めてみませんか?AMEDのwebサイトにも詳しい情報がありますので、ご覧ください。
‹›
ピックアップ:QMS/RBM
医療機関におけるQMS
この講座は、2020年12月12日に国立がん研究センター東病院で実施されたものです。GCP Renovationを目前に控え、医療機関における治験を実施する仕組み(プロセス)にも国際競争力を持った質の作りこみが求められる中、本邦において医療機関に求められているQMSとは何か、どうしたら品質マネジメントを向上することができるかをテーマに企画されたセミナーになります。
第2回 医療機関におけるQMS

この講座は、2021年5月22日に国立がん研究センター東病院で実施されたものです。GCP Renovationを目前に控え、医療機関における治験を実施する仕組み(プロセス)にも国際競争力を持った質の作りこみが求められる中、本邦において医療機関に求められているQMSとは何か、どうしたら品質マネジメントを向上することができるかをテーマに企画されたセミナーになります。
臨床研究・治験におけるQMSの概念に関する教育研修

この講座は、日本医療研究開発機構(AMED)令和5年度・6年度 研究開発推進ネットワーク事業 「地域、疾患領域、臨床研究者・支援専門職ネットワークを活用した、QMSの概念に関する研究者及び研究支援者への教育研修に係る研究(研究開発代表者:小居秀紀)」研究班の成果の一環として作成されたものです。Sponsor、Investigatorの役割を問わず、知識や経験が少ない初学者も含めた臨床研究に関わる全ての職種を対象に開催した「臨床研究・治験におけるQMSの概念に関するWebセミナー(令和6年1月22日開催) 」、並びに、所属する医療機関においてQMS・RBA推進のSponsorの役割の中核メンバーや、一部のInvestigatorの役割の中核メンバーの教育研修の場として開催した「研究者主導臨床研究・医師主導治験におけるQMSに基づくRBAの実装に関する集合研修(令和5年2月3日・4日開催) の内容となります。なお、本講座は動画作成において、NC・JIHS共通教育プラットフォーム事業の支援を一部受けています。
Risk-based approach(RBA)の実装に係る取組み
の実装に係る取組み.png)
この講座は、日本医療研究開発機構(AMED)臨床研究開発推進事業(医療技術実用化総合促進事業)の一環として、令和3年度の成果として作成されたものです。 ICH E6(R2)において、臨床試験の品質マネジメントシステム(Quality Management System QMS)、Risk Based Approach(RBA)の導入が明記されました。一方、研究者や研究支援者向けのRBA教育資材は限られていたのが現状です。この講座では、RBAの概念に始まり、医師主導治験を題材に治験開始前の重要なプロセス/データの特定やリスクの特定・評価・コントロール、治験実施中のリスクコミュニケーションやリスクレビュー、治験終了時のリスク報告まで体系的に学べるようになっています。
QMSの実装に向けたRBAの概念に関する教育研修
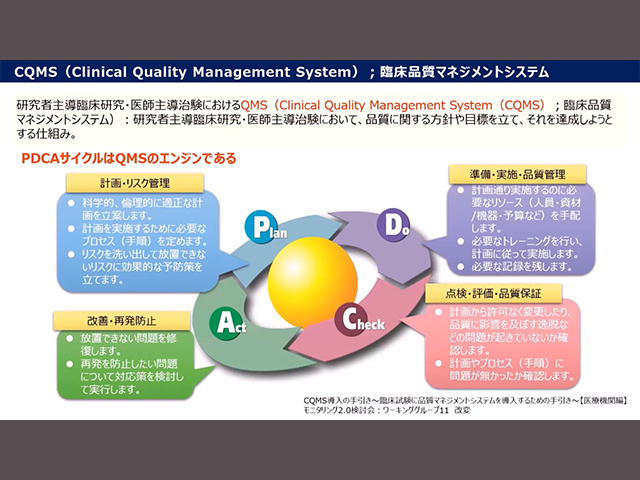
この講座は、日本医療研究開発機構(AMED)令和4年度 研究開発推進ネットワーク事業 「地域、疾患領域、臨床研究者・支援専門職ネットワークを活用した、QMSの実装に向けたRBAの概念に関する研究者及び研究支援者への教育資材の作成に資する研究」研究班の成果の一環として作成されたものです。臨床研究に関わる法令や倫理等の基礎知識はあるものの品質マネジメントに関する知識の習得が必要な臨床研究に関わる全ての職種を対象に、Sponsor、Investigatorの役割における立場別の観点も踏まえた、QMSの実装に向けたRBAの概念に関する研究者及び研究支援者への教育研修の場として、上記AMED研究班が主催した「Webセミナー(令和5年2月15日開催)」の内容となります。また、本講座は動画作成において、6NC共通教育プラットフォーム事業の支援を一部受けています。
RBA実装のための取り組み
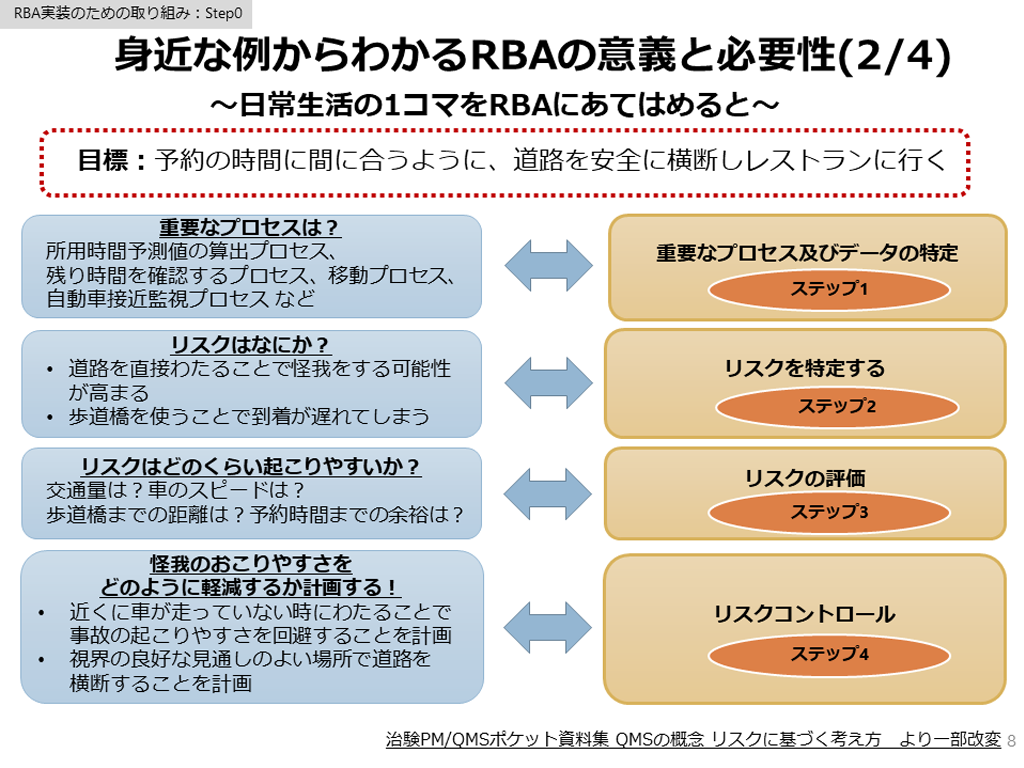
この講座では、日本医療研究開発機構(AMED)臨床研究開発推進事業(医療技術実用化総合促進事業)で作成した令和5年度の成果物を講義資料としてまとめた「e-learningコンテンツ」を掲載しています。ICH E6(R2)において、臨床試験の品質マネジメントシステム(Quality Management System QMS)、Risk Based Approach(RBA)の導入が明記されました。この講座は、研究者や研究支援者向けのRBA教育資材は限られていた中、2023年2月に公開し、その後、令和5年度までの事業成果を追加し改訂した最新の資料です。この講座では、RBAの概念に始まり、医師主導治験を題材に治験開始前の重要なプロセス/データの特定やリスクの特定・評価・コントロール、治験実施中のリスクコミュニケーションやリスクレビュー、治験終了時のリスク報告まで体系的に学べるようになっています。なお、RBAの手順書、説明書など本事業での成果物はAMEDホームページより参照できます(https://www.amed.go.jp/program/list/16/01/004_seika.html)。【本動画に関するお問い合わせ先】crc-kikaku@ml.chiba-u.jp(千葉大学病院RBA取りまとめ事務局)
研究者向け研究の品質管理とRBAの基礎

この講座は、日本医療研究開発機構(AMED)の研究開発推進ネットワーク事業の一環として、令和5~6年度の成果として作成されたものです。
RBA実践ガイド・事例集

本講座は、神戸医療産業都市推進機構 医療イノベーション推進センター 萩森奈央子を研究開発代表者とする国立研究開発法人日本医療研究開発機構(AMED)の「研究開発推進ネットワーク事業」に係る開発分野「臨床研究の質確保と効率的なマネジメントを目指したRBAの実装」において採択された研究課題「RBA実装事例の蓄積と臨床研究中核病院以外のAROにおいて効果的なRBA実装を可能とするためのツール整備」の成果物「効果的なRBA実装を可能とするためのツール」を掲載しています。ツールとして、実践にあたってのRBA手順への疑問点に対する解説やこれまでのRBAに関するAMED事業成果物の現場での使用方法の一例などを示しています。このツールは、皆様のRBA手順への理解が深まり、手順を進めることへのハードルが下がり、品質管理の本質を考える一歩となることを願って作成されました。
‹›
大橋靖雄先生特集
2021年3月に他界された中央大学理工学部教授大橋先生の講義を集めました臨床研究にかかわる人材の教育に熱心に取り組まれた大橋先生の熱い講義です。

0:36:53
PFSの再検討:がん進行タイプの解析が必要になるのか? 《講師:大橋靖雄》
がん臨床試験において重要なPFSやOSなどのエンドポイントについて、これまでの試験結果からの解釈だけでなく、問題点やOSとPFSの乖離の理由などさまざまな角度から解説いただきました。試験の結果を正確に理解するためにとても勉強になる内容となっております。
閲覧数1111
ユーザー評価4.15

00:57:36
がん臨床試験のエンドポイントはPFSかOSか? 《講師:大橋靖雄》
臨床試験デザインは年とともに変化しています。中でも、エンドポイントを何にするかというのは古くて新しい問題です。がんの臨床試験では、これまでOS(全生存期間)をプライマリ・エンドポイントにするのが一般的でしたが、近年、PFS(無増悪生存期間)を採用する試験が増えており、また、それに対する批判も多くあります。そこで、東京大学の大橋先生に、生物統計学だけでなく様々な観点から、最近の報告例を用いてその考え方を解説して頂きました。がんのみならず、QOLを含め、エンドポイントを何にするか考える際の根本的な考え方を学んでください。
閲覧数1958
ユーザー評価4.17

01:04:23
臨床試験における質とは何か? 《講師:大橋靖雄》
今回、「臨床試験における質とは何か?」をテーマに、統計家目線による講義です。この講義をきいて、質が高い臨床試験とは何か?どういった条件が必要か?ご自分でも考えてみましょう。
閲覧数1949
ユーザー評価4.13

00:16:30
日本臨床試験学会教育セミナー 総括 《講師:大橋靖雄》
本セミナー主催者である中央大学の大橋靖雄先生に当日のパネルディスカッションの内容とセミナー全体について総括して頂きました。パネルディスカッション自体はイーラーニングコンテンツとなっていませんので、ぜひご参照ください。
閲覧数1457
ユーザー評価3.95
‹›
ピックアップ:臨床試験デザイン
臨床研究を計画する際に何からどのように考えたらよいかは意外と難しいものです。対象、対照群、評価項目などをどのように考えていくかを中心に適切な研究デザインの方法についての基礎的な講義を集めました。

00:18:58
テーマ6:臨床試験の基礎知識③ -研究デザイン-
テーマ5では、「質の高いデータ」とはどのようなデータか、について学んでいただきました。その続きとして、この教材では、質の高いデータを得るための代表的な研究デザインについて解説します。 ※テーマ4~6では「臨床試験の基礎知識」を解説しています。順番にご受講いただくことをお勧めします。
閲覧数1714
ユーザー評価4.35
00:51:33
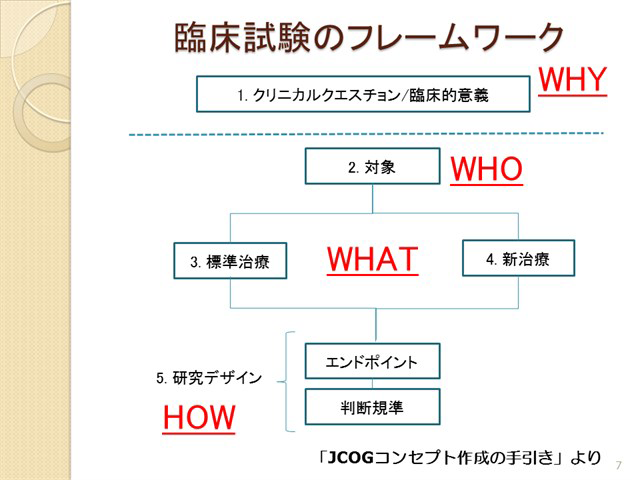
研究コンセプトの作り方-統計家の視点から-《講師:山本精一郎》
研究計画を立てる際には、プロトコールを作成する前に、研究の大まかの枠組みや重要な点、いわゆる研究コンセプトをしっかりと作成することが必要です。本講義ではPICOに代表される一般的な研究コンセプトのフレームワークを解説するだけでなく、具体的な研究を例にして実際にどのように対象・治療・エンドポイントを決定していくかをわかりやすく説明しています。 本講義をご覧頂いた後に、福田治彦先生の「コンセプトの作り方」を受講頂くとさらに理解が深まります。是非受講ください。
閲覧数13179
ユーザー評価4.26
01:01:06
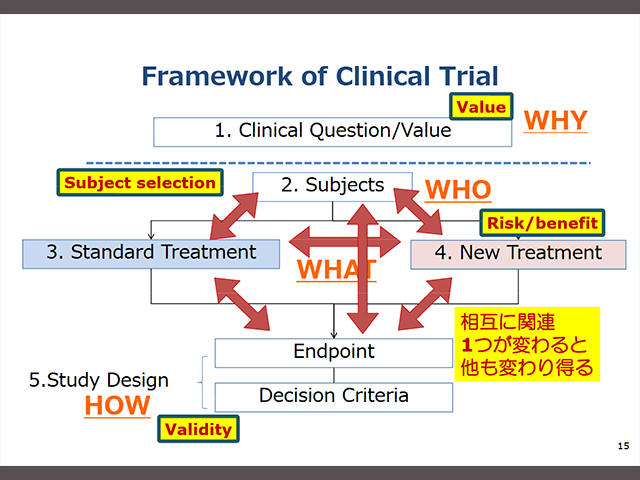
コンセプトの作り方 《講師:福田治彦》
本講義は、がんの多施設共同臨床試験グループJCOGの主催する、第18回JCOG臨床試験セミナー(中級編)で2015年10月10日に行われた講義を収録したものです。臨床試験のプロトコールコンセプトの作り方について説明しています。プロトコールコンセプトとは、臨床研究計画書(プロトコール)のサマリーです。研究計画を立てる段階では、プロトコールを作成する前に、コンセプトを作成することが非常に有用です。本講義では、コンセプトのフレームワークを紹介し、「人を対象とする医学系研究に関する倫理指針」の「目的及び基本方針」に記載された臨床研究の原則である、社会的/科学的価値、科学的妥当性、適正な被験者選択、適切なリスク/ベネフィットバランス、などをいかに研究計画に反映するかを説明しています。実例を元にして、コンセプトの作成のポイントを丁寧に解説しておりますので、ぜひ研究計画の質の向上に活かして下さい。
閲覧数3601
ユーザー評価4.16
01:45:00
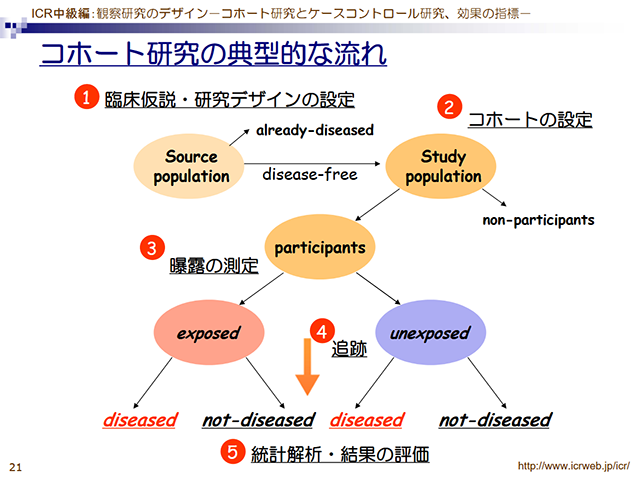
観察研究のデザイン-コホート研究とケース・コントロール研究、効果の指標- 《講師:吉村健一》
コホート研究とケースコントロール研究についてご紹介します。これらの研究デザインとその効果の指標は病気の原因を調べるために用いられることが多いのですが、レトロの研究での治療評価や予後因子評価にも用いられます。
閲覧数2654
ユーザー評価4.08
‹›
レギュラーコース
GCPトレーニング(R2対応版)
.png)
本講座は治験に係わる前に必要とされるGCP トレーニングとして作成いたしました。本プログラムはv1.0が2016年2月にTransCelerateによって認定されました。そのため、治験用の公式プログラムとしてご利用いただいております。また、ICH-GCP E6(R2)への改訂に伴い本プログラムも改定し、v2.0として2017年10月にTransCelerateに承認されました。そのため、最新のトレーニングの受講と修了証を希望の方はこちらのver2.0を受講ください。公式プログラムとして利用は可能ですが、実際に治験用に利用される場合には、各企業にご確認の上、ご利用ください。なお、R3対応についての問い合わせを数多くいただいております。掲載を予定しておりますが、現時点で時期は未定です。
JCOG臨床試験セミナー 入門編
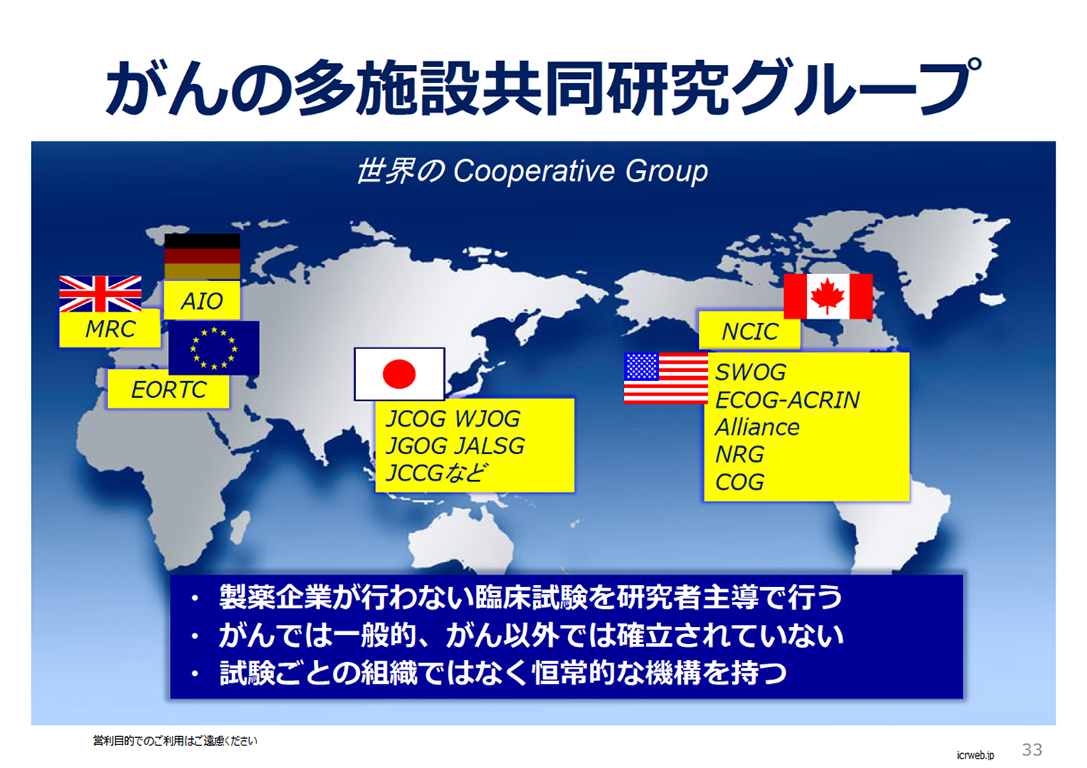
この講座では、臨床試験を行う際に必要な考え方を学習します。本講座は、がんの多施設臨床試験グループである日本臨床腫瘍研究グループ(JCOG)が臨床試験に関与し始めたばかりの医師や、臨床研究の支援スタッフ向けに2022年10月8日に開催したセミナーを収録したものです。臨床試験の基本的な考えを説明していますから、自分の分野に当てはめて考え、その考え方を学んでください。過去、大変好評であったJCOG臨床試験支援するCRCによる「JCOG参加施設のCRCによる臨床試験支援1、2、3」は引き続き掲載していますので参考にしてください。本講座は「令和4年度AMED臨床研究・治験推進研究事業(生物統計家育成推進事業)」により作成されました。
生物統計基礎セミナー
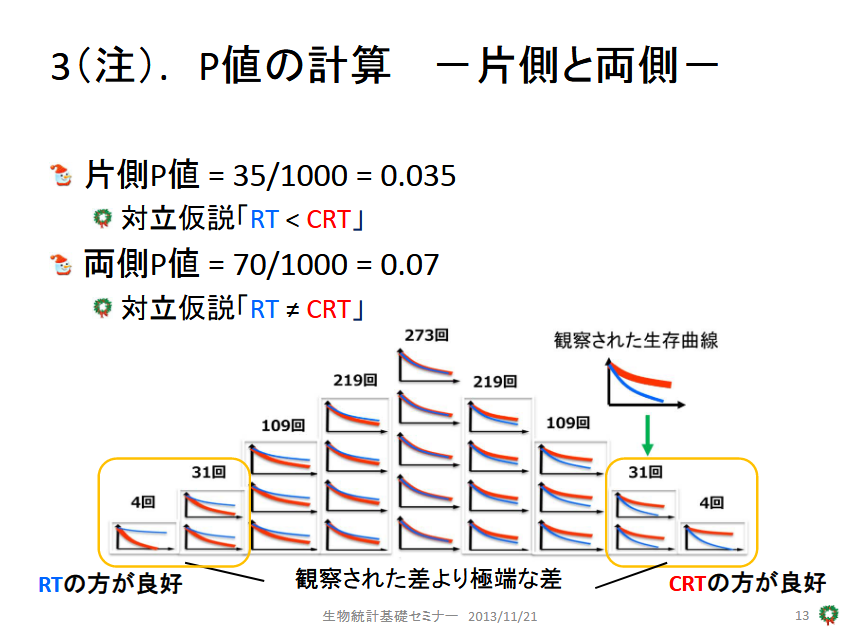
臨床研究(看護研究、疫学研究などを含む)を自ら実施する研究者が知っておくべき、生物統計学・疫学の方法論および考え方を提供する講座です。介入研究・観察研究のどちらにも求められる概念を説明します。統計ソフトの使い方などの単なるクックブックではなく、自分自身で研究の計画・結果の解釈・批判的吟味ができるようになることを目標としています。
倫理審査委員向けの倫理研修用動画教材(東京大学作成)

REC EDUCATIONプログラムは、AMED「平成28年度 研究公正高度化モデル開発支援事業」において倫理審査委員の倫理研修用に制作されたもので、倫理審査に必要な基礎的知識を身につけることができます。倫理審査委員会開催に際して利用しやすいよう、1テーマ20分程度で構成されています。(同プログラムはAMED「平成31年度 研究公正高度化モデル開発支援事業」でも継続しています。 詳しくは、「 REC EDUCATION - ▼ 倫理審査委員用サイト」をご覧ください) 主な対象者:倫理審査委員、倫理審査委員会事務局
NC・JIHS:臨床研究講座(NCC)

本講座では国立がん研究センター(NCC)の臨床研究に関する講義で構成されます。各がん種の治療開発だけでなく、臨床研究の方法論やQMS、規制関連(GCP、指針、先進医療と患者申出療養)、その他DCTやQMSなどの最新のトピックスなどを公開していきます。
NC・JIHS:臨床研究講座(JIHS)

本講座では国立健康危機管理研究機構(JIHS)で収録された臨床研究に関する講義で構成されます。
NC・JIHS:情報セキュリティ対策講座(JIHS)

本講座は医療機関へのサイバー攻撃等への対策を立てるために必要な知識を学ぶための講義から構成されます。講義はJIHSの医療情報センターのメンバーにより収録されました。
NC・JIHS:Office365利用による業務効率化講座(JIHS)

すべてのNCおよびJIHSは業務にOffice365を使用している。Office365は医療機関における事務作業の自動化に役立つ多くの便利機能(アプリ)が備わっている。本講座ではJIHS内での利用事例の紹介と自動化を行うためのアプリの使用方法を解説する。
NC・JIHS:リピドミクス講座(JIHS)

本講座でリピドミクス研究に関する5講義から構成されます。講義には、リピドミクスとは何か(概論)、分析方法、医療研究への応用等が含まれているます。これからリピドミクスの初心者にも分かりやすい内容となっています。
NC・JIHS:薬剤耐性(AMR)講座(JIHS)

本講座は国立健康危機管理研究機構(JIHS)で収録された薬剤耐性(AMR)に関する講義で構成されます。
NC・JIHS:循環器疾患講座(NCVC)

本講座では国立循環器病研究センター(NCVC)で収録された循環器疾患研究に関する講義で構成されます。
NC・JIHS:うつ病講座(NCNP)

本講座は国立精神・神経医療研究センター(NCNP)のうつ病等の精神疾患に関する講義で構成されます。
NC・JIHS:臨床研究モニタリングとデータマネジメント講座(NCNP)

本講座は国立精神・神経医療研究センター(NCNP)の臨床研究に関する講義で構成されます。
NC・JIHS:小児医療研究講座(NCCHD)

本講座は国立成育医療研究センター(NCCHD)の小児医療研究に関する講義で構成されます。
NC・JIHS:認知症講座(NCGG)

本講座は国立長寿医療研究センター(NCGG)で作成された認知症に関する講義で構成されています。認知症の診断や予防、認知症のリスク等に関する最新の研究について学習ができます。
NC・JIHS:臨床研究講座(NCGG)
本講座は国立長寿医療研究センター(NCGG)で収録された臨床研究に関する講義で構成されます。
NC・JIHS:動物実験講座

本講座は「厚生労働省の所管する実施機関における動物実験等の実施に関する基本指針」に定められた教育訓練に必要なコンテンツを中心に構成されています。5つのNCおよびJIHSの実験動物管理室が連携して作成し、1つのコンテンツが15~30分程度の聴講しやすい講義にしています。また、実験動物福祉に配慮するべき動物実験処置の苦痛度分類、人道的エンドポイントの設定、実験動物の麻酔法など、重要な項目については、細分化して丁寧かつ詳細に解説しています。是非、このコンテンツを有効に活用していただければ幸いです。
NC・JIHS:知的財産セミナー

本講座は医療研究で身につけておくべき知的財産に関する基礎知識に関する講義で構成されます。ナショナルセンター医療研究連携推進本部 (Japan Health Research Promotion Bureau:JH)知財・法務課が作成しました。
NC・JIHS:データサイエンス研修(NCCHD)

本講座は国立成育医療研究センター(NCCHD)のデータサイエンス研修に関する講義シリーズで構成されます。NCCHDでは2018年のAIホスピタル事業採択を機に、研究者、医師だけでなく、全ての職員を対象としたデータサイエンスの教育活動を行なっています。独自の研修方針で仲間を募り、特にコロナ禍を経て教育用動画の作成も行ってきました。2022年、ICRwebからこれらの動画を公開していただくことになり、データサイエンス研修とそこで作られている動画について紹介させていただきます。
生物統計発展セミナー
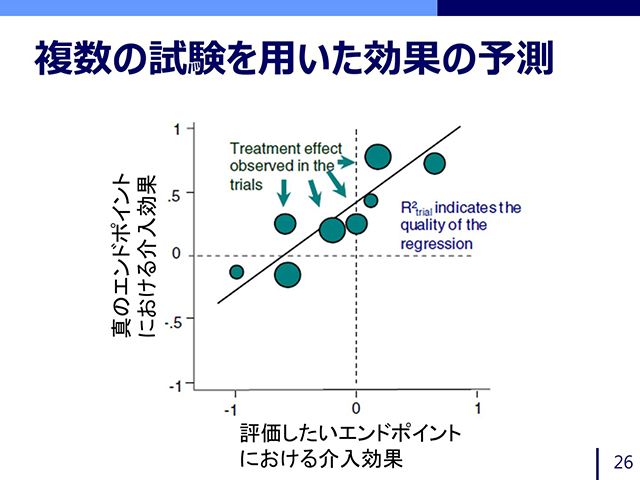
生物統計基礎セミナーの内容を超えた発展的な内容や、一つのトピックをより深堀した内容をまとめた講座です。生物統計基礎セミナーの内容はある程度理解できていることを前提としています。
因果推論入門講座
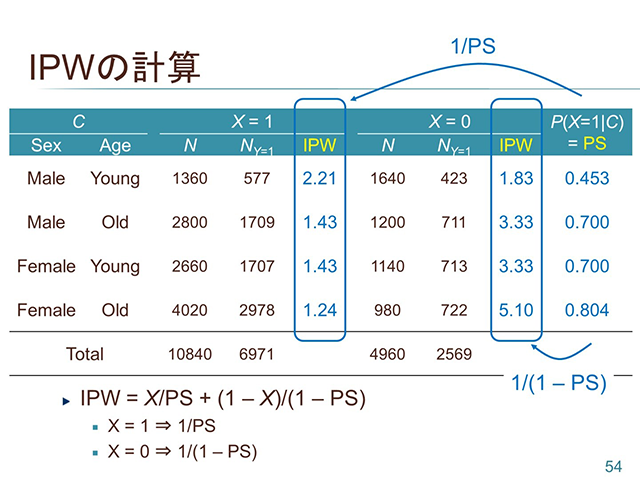
この講座は因果推論の入門講座です。欠測データに対する取り扱いの問題に対する議論が活発になり、またリアルワールドデータなどのレジストリや観察研究のデータの利用が注目される中、因果推論に関する基礎知識の習得が求められるようになりつつあります。「因果推論って何?」という方も、「言葉だけは知っているけど良くわからない」という方も、誰にでもわかりやすく入門的な内容をわかりやすく解説した講義です。
臨床研究の方法論的トピック
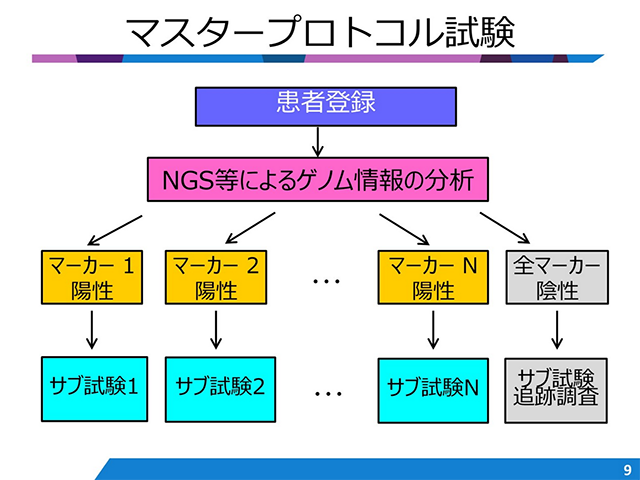
この講座では、臨床研究で時々遭遇するトピックについて、様々な話題を提供します。
臨床研究のデータマネージメント入門講座1
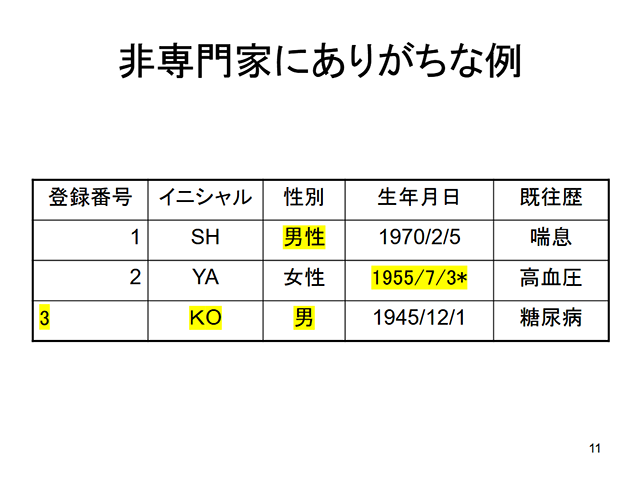
この講座は、臨床研究のデータマネージメントについての基本的な考え方をまとめた講座です。データマネージメントに関与し始めたばかりのデータマネジャーや、データマネジャー以外の専門職の方、治験や臨床試験において中央支援機構のデータマネジャーがどのようなことをしているのか興味・関心のある方は是非ともご覧ください。
PRO/QOL 評価を組み込んだ臨床試験の実践

Patient Reported Outcome(PRO)とは臨床研究のアウトカムのうち、患者自身が病気や治療などに関する評価を行い、医師などの他の者が別の解釈を加えないものを言います。近年、患者さんの声を治療開発に活かすことや医療経済評価を目的として、PRO形式でQOLを評価することが増えつつありますが、一方でPRO/QOLを用いた臨床研究の計画、評価は難しく、わからないことが多いと思います。本シンポジウムはPRO/QOLを用いた臨床研究をやってみたいけれど、やり方が良くわからない方を対象に、基礎的な網羅的に解説しています。興味のある方は「 EORTC-JCOG PRO/QOLワークショップ2018講座」も合わせてご覧ください。本講座は「2021年度AMED清田班シンポジウム 《PRO/QOL 評価を組み込んだ臨床試験をやってみよう!!》」を収録したものです。
‹›